Le lait, un aliment fondamental dans de nombreuses cultures, est une substance complexe dont la qualité est influencée par une multitude de facteurs. Parmi ceux-ci, son acidité joue un rôle crucial, affectant sa saveur, sa durée de conservation, et son aptitude à la transformation. La mesure précise de cette acidité est donc une étape indispensable dans l'industrie laitière, de la ferme à la production de produits finis. C'est ici qu'intervient le pHmètre, un instrument de précision permettant de quantifier le niveau d'acidité du lait.

Comprendre l'Acidité du Lait : Un Concept Clé
L'acidité du lait, souvent exprimée en degrés Dornic (°D), est principalement due à la présence d'acide lactique, un produit de la fermentation du lactose par des bactéries lactiques. Cependant, d'autres composants du lait contribuent également à son acidité, notamment les phosphates, les citrates, le dioxyde de carbone dissous, et les protéines. L'acidité titrable, mesurée par une titration avec une base forte (comme l'hydroxyde de sodium), reflète la somme de tous ces composants acides. L'acidité active, quant à elle, est directement liée à la concentration en ions hydrogène (H+), et c'est cette dernière que le pHmètre mesure.
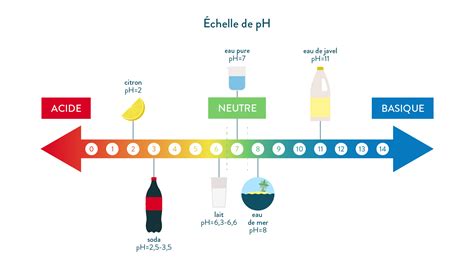
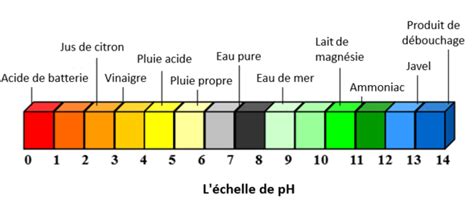
Le pH est une échelle logarithmique qui indique la concentration en ions hydrogène. Un pH de 7 est considéré comme neutre. Les valeurs inférieures à 7 indiquent une acidité (plus le pH est bas, plus le milieu est acide), tandis que les valeurs supérieures à 7 indiquent une alcalinité. Le lait frais, idéalement, a un pH compris entre 6,6 et 6,8. Une diminution de ce pH est un indicateur précoce de détérioration ou de développement bactérien indésirable.
Le pHmètre : Principe de Fonctionnement et Calibration
Le pHmètre est un appareil électronique conçu pour mesurer le potentiel hydrogène d'une solution. Il est généralement composé d'une électrode sensible aux ions hydrogène et d'un appareil de mesure qui affiche la valeur du pH. L'électrode, souvent une électrode de verre, fonctionne sur le principe d'un potentiel électrique généré à travers une membrane de verre en fonction de la différence de concentration en ions H+ entre la solution à mesurer et une solution interne de référence. Ce potentiel est ensuite converti en une lecture de pH par l'appareil.
Pour garantir des mesures fiables et précises, la calibration du pHmètre est une étape absolument fondamentale. Cette calibration consiste à ajuster l'appareil pour qu'il fournisse des lectures correctes en utilisant des solutions tampons de pH connu. Typiquement, on utilise au moins deux solutions tampons, dont les pH sont proches de la plage de mesure attendue pour le lait. Les solutions tampons couramment utilisées sont le tampon pH 4, le tampon pH 7 et le tampon pH 10.
Le processus de calibration implique généralement les étapes suivantes :
- Rinçage de l'électrode : L'électrode est rincée à l'eau distillée ou désionisée pour éliminer tout résidu de la solution précédente.
- Immersion dans le premier tampon : L'électrode est immergée dans la première solution tampon (par exemple, pH 7). L'appareil est ensuite ajusté pour afficher la valeur correcte du tampon.
- Rinçage et séchage : L'électrode est à nouveau rincée et délicatement séchée.
- Immersion dans le second tampon : L'électrode est immergée dans la seconde solution tampon (par exemple, pH 4). L'appareil est ajusté pour afficher la valeur correcte de ce second tampon.
- Vérification : Il est parfois recommandé de vérifier la calibration en immergeant l'électrode dans un troisième tampon ou dans une solution de contrôle.
Une calibration régulière, idéalement avant chaque série de mesures importantes, est essentielle car la sensibilité de l'électrode peut varier avec le temps, la température et l'usage. L'état de l'électrode (propreté, absence de fissures) influence également la précision de la mesure.
Tuto rapide : Comment calibrer le PH-80 de HM Digital pour des mesures précises ?
La Mesure du pH du Lait : Procédure et Interprétation
Une fois le pHmètre correctement calibré, la mesure du pH du lait peut être effectuée. La procédure est relativement simple :
- Préparation de l'échantillon : Le lait doit être homogénéisé pour assurer une distribution uniforme des composants. Il est important que le lait soit à une température stable, car la température affecte la lecture du pH. La plupart des pHmètres modernes disposent d'une compensation de température automatique (ATC), mais il est toujours bon de connaître la température de l'échantillon. Idéalement, la mesure doit être effectuée à température ambiante ou à une température standardisée.
- Immersion de l'électrode : L'électrode du pHmètre, préalablement rincée et séchée, est immergée dans l'échantillon de lait, en veillant à ce que la partie sensible de l'électrode soit complètement recouverte.
- Stabilisation de la lecture : Il faut attendre que la lecture du pHmètre se stabilise. Cela peut prendre quelques instants, le temps que l'électrode réagisse complètement à la composition du lait.
- Enregistrement de la valeur : Une fois la lecture stable, la valeur du pH est enregistrée.
L'interprétation des résultats est cruciale pour évaluer la qualité du lait :
- Lait frais : Un pH entre 6,6 et 6,8 indique un lait de bonne qualité, avec une activité bactérienne normale.
- Lait légèrement acide : Un pH entre 6,4 et 6,6 peut suggérer le début d'une activité bactérienne accrue ou une légère altération.
- Lait acide : Un pH inférieur à 6,4 indique une acidité élevée, souvent due à une fermentation lactique avancée. Cela peut être le signe d'une mauvaise hygiène, d'une température de stockage inadéquate, ou d'une contamination bactérienne importante. Un tel lait peut avoir un goût aigre et une durée de conservation réduite. Il peut également poser des problèmes lors de la fabrication de produits laitiers, comme la coagulation du lait lors de la production de fromage.
- Lait alcalin : Un pH supérieur à 6,8 est moins courant pour le lait frais et peut indiquer la présence de colostrum (le premier lait produit après la mise bas, qui est naturellement plus alcalin), ou une contamination par des micro-organismes produisant des alcalis, ou encore une dilution avec de l'eau.
L'Importance de la Mesure du pH dans l'Industrie Laitière
La mesure du pH du lait par pHmètre étalonné est une pratique incontournable à plusieurs niveaux de la chaîne de production laitière :
- Contrôle à la ferme : Les producteurs laitiers utilisent des pHmètres pour surveiller la qualité du lait avant même qu'il ne quitte la ferme. Cela permet d'identifier rapidement les problèmes potentiels liés à l'hygiène, au stockage ou à la santé des animaux.
- Réception du lait : Les laiteries et les transformateurs de produits laitiers effectuent des contrôles de pH à la réception du lait pour s'assurer qu'il répond aux normes de qualité requises. Un lait trop acide peut être refusé ou utilisé pour des applications moins valorisées.
- Fabrication de produits laitiers : Dans la fabrication de produits tels que le fromage, le yaourt, le kéfir ou la crème aigre, le contrôle précis du pH est essentiel pour maîtriser le processus de fermentation et obtenir les caractéristiques organoleptiques désirées. Par exemple, dans la fabrication du fromage, le pH influence la coagulation des protéines du lait et la texture du produit final.
- Surveillance de la durée de conservation : La mesure du pH peut aider à évaluer la fraîcheur du lait et à prédire sa durée de conservation. Une augmentation de l'acidité au fil du temps est un signe de dégradation.
L'utilisation d'un pHmètre étalonné garantit que ces mesures sont fiables et reproductibles, fournissant ainsi des données précieuses pour la prise de décision et le maintien d'une haute qualité des produits laitiers. Ignorer l'importance de la calibration ou négliger la mesure du pH peut entraîner des pertes économiques, des problèmes de qualité des produits, et une insatisfaction des consommateurs. La technologie du pHmètre, associée à une procédure rigoureuse, reste donc un pilier du contrôle qualité dans l'industrie laitière.